- Auteur Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:46.
- Laatst gewijzigd 2025-01-23 11:15.
Belangrijk verschil - Alifatische versus aromatische koolwaterstoffen
Laten we eerst kort zien welke koolwaterstoffen het verschil tussen alifatische en aromatische koolwaterstoffen bespreken. Koolwaterstoffen zijn de organische verbindingen die koolstof- en waterstofatomen in hun structuur bevatten. Het belangrijkste verschil tussen alifatische en aromatische koolwaterstoffen is dat alifatische koolwaterstoffen geen geconjugeerd bindingssysteem bevatten, terwijl aromatische koolwaterstoffen een geconjugeerd bindingssysteem bevatten. Beide moleculen worden echter als organische verbindingen beschouwd.
Wat zijn alifatische koolwaterstoffen?
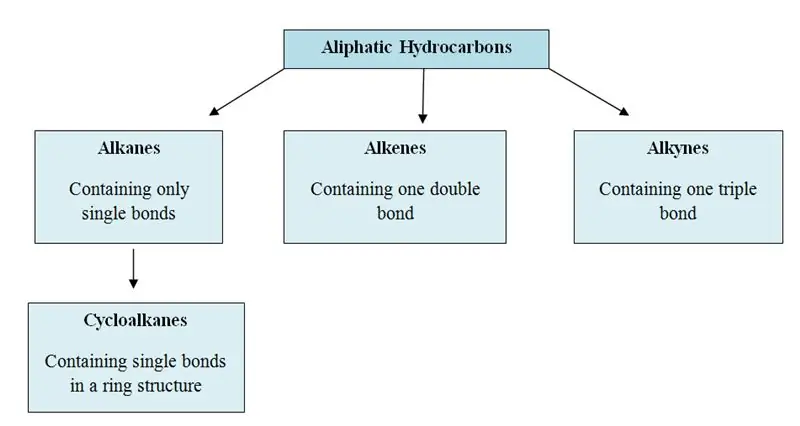
Alifatische koolwaterstoffen zijn de organische moleculen die koolstof (C) en waterstof (H) atomen in hun structuur bevatten; in rechte ketens, vertakte ketens of niet-aromatische ringen. Alifatische koolwaterstoffen kunnen worden onderverdeeld in drie hoofdgroepen; alkanen, alkenen en alkynen.
Wat zijn aromatische koolwaterstoffen?
Aromatische koolwaterstoffen zijn soms bekend als "arenen" of "arylkoolwaterstoffen". De meeste aromatische koolwaterstoffen bevatten een benzeenring in hun structuur; maar er zijn niet-benzeen aromatische koolwaterstoffen die heteroarenen worden genoemd en die de " regel van Huckle " volgen (cyclische ringen die de regel van Huckle volgen hebben 4n + 2 aantal π-elektronen; waarbij n=0, 1, 2, 3, 4, 5, 6). Sommige aromatische koolwaterstoffen hebben meer dan één ring; ze worden polycyclische aromatische koolwaterstoffen genoemd.
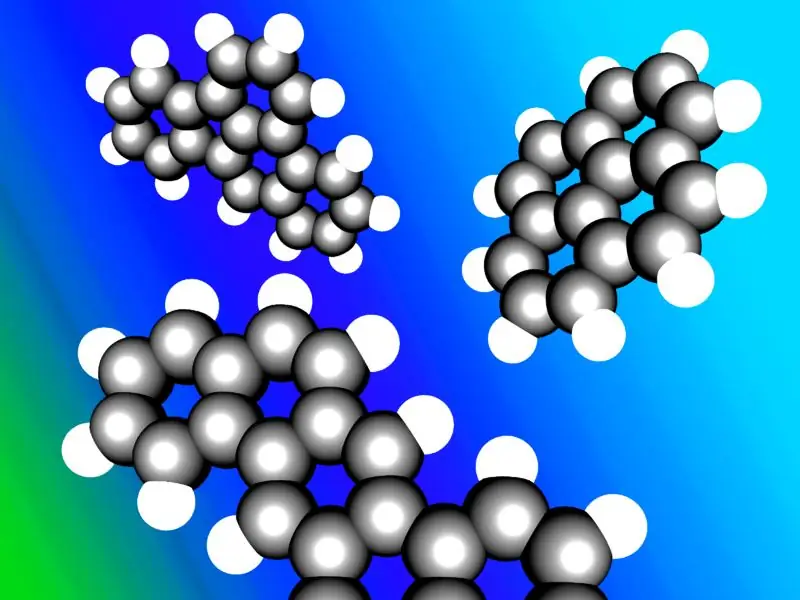
Een illustratie van typische polycyclische aromatische koolwaterstoffen.
Wat is het verschil tussen alifatische en aromatische koolwaterstoffen?
Structuur van alifatische en aromatische koolwaterstoffen
Alifatische koolwaterstoffen: ze hebben rechte ketens, vertakte ketens of niet-aromatische ringen in hun structuur. Deze groep heeft zowel verzadigde als onverzadigde koolwaterstoffen. Alkanen zijn verzadigde koolwaterstoffen, alkenen en alkynen zijn onverzadigde koolwaterstoffen.
Rechte Kettingen:
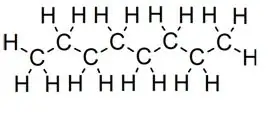
Octane
Branded Chains:
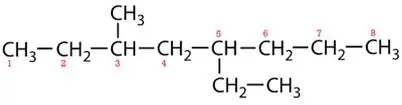
5-ethyl-3-methyloctaan

2-methyl-3-pentence
Niet-aromatische ringen:
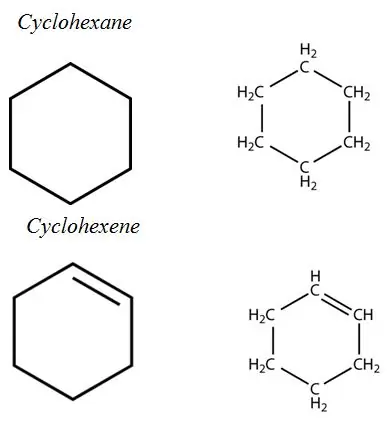
Aromatische koolwaterstoffen: Aromatische koolwaterstoffen hebben een aromatisch ringsysteem in hun structuur. Het zijn allemaal onverzadigde koolwaterstoffen, maar relatief stabiel dankzij het geconjugeerde bindingssysteem.
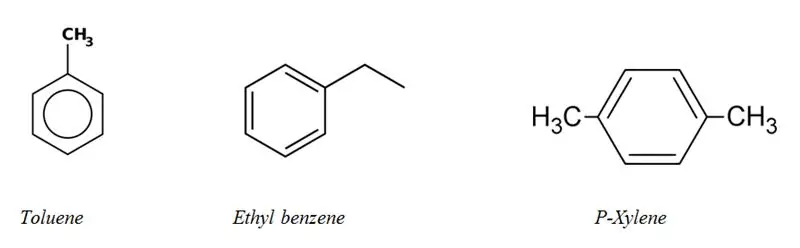
Categorieën van alifatische en aromatische koolwaterstoffen
Alifatische koolwaterstoffen:
Er zijn drie hoofdgroepen in alifatische koolwaterstoffen; alkanen, alkenen en alkynen. Ze zijn ook bekend als allylkoolwaterstoffen.
Alkanen: In alkanen zijn koolstof- en waterstofatomen aan elkaar gebonden door enkele bindingen. Ze hebben geen meerdere bindingen. Alkanen vormen ringstructuren, ze worden cycloalkanen genoemd.
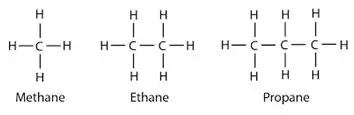
Alkenen: Deze groep bevat zowel enkele als dubbele bindingen tussen koolstofatomen. Waterstof- en koolstofatomen vormen altijd enkelvoudige bindingen.
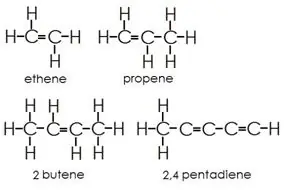
Alkynen: Alkynen hebben drievoudige bindingen tussen koolstofatomen naast enkele bindingen.
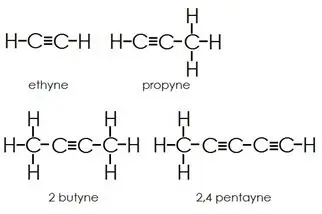
Aromatische Koolwaterstoffen:
De meeste aromatische koolwaterstoffen bevatten ten minste één benzeenring in hun structuur. Maar er zijn weinig niet-benzeen aromatische koolwaterstoffen, ze worden "heteroarenen" genoemd. Aromatische koolwaterstoffen worden "aryl"-koolwaterstoffen genoemd.
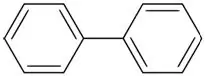
Bifenyl (Een aromatische koolwaterstof met twee benzeenringen)
Verbindingspatroon van alifatische en aromatische koolwaterstoffen
Alifatische koolwaterstoffen:
In alifatische koolwaterstoffen; enkele, dubbele of driedubbele bindingen kunnen overal in het molecuul voorkomen. Soms kunnen er meerdere structuren zijn voor één molecuulformule door de positie van de meervoudige binding(en) te veranderen. Deze moleculen hebben een gelokaliseerd elektronensysteem.
Aromatische Koolwaterstoffen:
In aromatische koolwaterstoffen hebben ze een alternatief systeem met enkele en dubbele binding om een geconjugeerd bindingssysteem te vormen om sommige elektronen te delokaliseren. (Gedelokaliseerde elektronen kunnen van de ene binding naar de andere gaan).
Reacties van alifatische en aromatische koolwaterstoffen
Alifatische koolwaterstoffen:
Verzadigde koolwaterstoffen ondergaan substitutiereacties; onverzadigde koolwaterstoffen bereiken de stabiliteit door additiereactie. Maar sommige reacties vinden plaats onder gecontroleerde omstandigheden zonder meerdere bindingen te verbreken.
Aromatische Koolwaterstoffen:
Aromatische koolwaterstoffen zijn onverzadigd, maar hebben een stabiel geconjugeerd elektronensysteem, zodat ze meer vatbaar zijn voor substitutiereacties dan voor additiereacties.
Image Courtesy: "Polycyclic Aromatic Hydrocarbons" door Inductiveload - Eigen werk van uploader, Accelrys DS Visualizer. (Public Domain) via Commons






